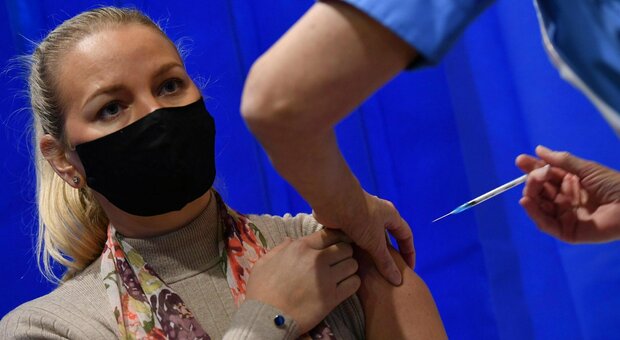
Un piccolo stop al vaccino. L'autorità nazionale di controllo sui farmaci (Mhra) ha raccomandato oggi di non sottoporre a vaccinazione anti Covid chi abbia alle spalle una storia di «significative» reazioni allergiche. L'indicazione è arrivata dopo che due delle centinaia di persone a cui è stato somministrato il vaccino Pfizer/Biontech nel Regno Unitio - primo Paese ad aver dato il via ieri alla distribuzione pubblica, dopo il via libera dato nei giorni scorsi dalla stessa Mhra - hanno avuto reazioni allergiche.
Covid, Pregliasco: «Terza ondata è fatto quasi certo, numero di decessi incredibile»
People with a history of “significant” allergic reactions have been told to refrain from the Pfizer Covid vaccine after two NHS nurses became unwell.
— The Times (@thetimes) December 9, 2020
The step is a precaution, and no-one from the 43,000-person trails experienced such reactions. https://t.co/bjKgO22lu7
Le persone colpite da reazione allergica nella prima giornata di vaccinazione sono due operatori sanitari di case di cura e ricovero vaccinati nella prima categoria di priorità assieme a un contingente iniziale di degenti ultraottantenni di queste strutture, ha poi confermato il servizio sanitario nazionale dell'Inghilterra (Nhs England). Non senza precisare che tutti gli ospedali coinvolti nella distribuzione del vaccino Pfizer sono stati avvertiti dell'accaduto e informati della raccomandazione della Mhra di evitare la somministrazione a chi abbia avuto in passato episodi seri di allergia.
Vaccino Covid, gli Emirati Arabi registrano quello cinese: efficace all'86%
Si tratta di procedure standard, ha poi minimizzato il professor Stephen Powis, direttore medico dell'Nhs in Inghilterra osservando come sia «comune che la Mhra suggerisca cautele in caso di nuovi vaccini per le persone con una storia significativa di allergie». Powis ha inoltre assicurato che i due sanitari dell'Nhs andati incontro ieri a reazioni di questo tipo dopo la vaccinazione anti Covid non sono in gravi condizioni e «stanno entrambi riprendendosi bene». Il vaccino è stato «ben tollerato» durante la sperimentazione e non è al centro di alcuna «preoccupazione seria di sicurezza», ha inoltre confermato una portavoce della stessa Pfizer. La portavoce ha tra l'altro ricordato che la sperimentazione di questo prototipo è stata condotta in totale finora su «44.000 partecipanti, 42.000 dei quali hanno ricevuto già la seconda dose del vaccino».
Intanto, anche il Canada ha dato il via libera al vaccino della Pfizer, diventando il secondo Paese dopo il Regno Unito, ed il co-fondatore di Biontech Ugur Sahin ha annunciato che la seconda generazione del vaccino di Pfizer-Biontech potrebbe essere pronta già nella seconda metà del 2021: l'azienda è già al lavoro sul nuovo vaccino, che potrebbe essere trasportato a temperatura ambiente, piuttosto che agli attuali -70 gradi, condizione che rende il trasporto logisticamente complicato.
Emirati arabi
Gli Emirati arabi uniti hanno infatti registrato il vaccino sperimentale della cinese Sinopharm la cui efficacia s'è attestata all'86% contro il Covid-19, in base a un'analisi provvisoria dei test di fase 3 iniziati a luglio. Confermata anche l'efficacia del vaccino AZD1222, sviluppato da AstraZeneca e dall'Università di Oxford con Irbm di Pomezia: lo studio relativo alla finale fase 3 è stato pubblicato sulla rivista Lancet e si tratta della prima azienda che pubblica i risultati finali di un candidato vaccino su una rivista secondo il meccanismo della revisione paritaria dei dati (peer-review). I risultati pubblicati confermano che il vaccino ha un'efficacia del 62,1% se somministrato in due dosi intere, e del 90% nei volontari che hanno ricevuto mezza dose seguita da una dose intera (l'efficacia media è del 70%). Il vaccino è risultato efficace nel prevenire la malattia Covid-19, senza casi gravi e senza ricoveri oltre 21 giorni dopo la prima iniezione.
Agenzia italiana del farmaco
Quanto alle presunte date in cui il vaccino di Pfizer/Biontech potrebbe essere disponibile per la somministrazione in Italia, «ancora non c'è una tempistica precisa per l'inizio delle vaccinazioni in Italia. La data è legata ai tempi di autorizzazione dell'Agenzia Europea dei Medicinali (Ema) e la validazione italiana sarà pressoché immediata rispetto a quella europea ma, ad ora, non ci sono basi per indicare un giorno preciso rispetto a un altro», fa sapere l'Agenzia Italiana del Farmaco (Aifa).
Vaccino, Cooke (EMA): giudizio su Pfizer 29 dicembre, su Moderna 12 gennaio
Ultimo aggiornamento: Mercoledì 30 Dicembre 2020, 12:50
© RIPRODUZIONE RISERVATA