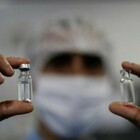
La (terza) dose addizionale di vaccino anti-Covid (booster) deve essere somministrata dopo almeno 28 giorni dalla seconda dose. Per dose addizionale si intende una dose aggiuntiva a completamento del ciclo vaccinale primario, per raggiungere un adeguato livello di risposta immunitaria. Si parte dai pazienti trapiantati. Gianni Rezza, dg del Ministero della Salute ha emanato la circolare contenente "indicazioni preliminari sulla somministrazione di dosi addizionali e di dosi “booster” nell’ambito della campagna di vaccinazione anti SARS-CoV-2/COVID-19".
Terza dose vaccino a 28 giorni dall'ultima iniezione: si parte dai trapiantati. Le dieci categorie
Regione Lazio, D'Amato: «Terza dose vaccino? Stiamo già reclutando trapiantati»
La circolare della salute in formato .pdf
La circolare del Ministero
Secondo a quanto prescritto dalla circolare che ha alcuni allegati, sono dieci le categorie di pazienti che potranno ricevere la terza dose 'addizionale' di vaccino anti-Covid (le categorie potranno essere aggiornate sulla base di evidenze disponibili):
- trapianto di organo solido in terapia immunosoppressiva;
- trapianto di cellule staminali ematopoietiche (entro 2 anni dal trapianto o in terapia immunosoppressiva per malattia del trapianto contro l'ospite cronica);
attesa di trapianto d'organo;
- terapie a base di cellule T esprimenti un Recettore Chimerico Antigenico (cellule CART);
patologia oncologica o onco-ematologica in trattamento con farmaci immunosoppressivi, mielosoppressivi o a meno di 6 mesi dalla sospensione delle cure; immunodeficienze primitive (es. sindrome di DiGeorge, sindrome di Wiskott-Aldrich, immunodeficienza comune variabile etc.);
- immunodeficienze secondarie a trattamento farmacologico (es: terapia corticosteroidea ad alto dosaggio protratta nel tempo, farmaci immunosoppressori, farmaci biologici con rilevante impatto sulla funzionalità del sistema immunitario etc.);
- dialisi e insufficienza renale cronica grave;
- pregressa splenectomia;
- sindrome da immunodeficienza acquisita (AIDS) con conta dei linfociti T CD4+ < 200cellule/µl o sulla base di giudizio clinico.
Sulla base delle indicazioni fornite in precedenza, questi soggetti dovrebbero aver già ricevuto due dosi di vaccino a m-RNA.
Le indicazioni del Cts
Al momento, in base alle indicazioni del CTS, si considera prioritaria la somministrazione della dose addizionale nei soggetti trapiantati e immunocompromessi. Ferma restando la priorità del raggiungimento di un'elevata copertura vaccinale con il completamento dei cicli attualmente autorizzati, sarà definita la strategia di somministrazione di una dose “booster” di vaccino a m-RNA (Comirnaty di BioNTech/Pfizer e Spikevax di Moderna) in favore di ulteriori gruppi target, a cominciare da quelli sopra menzionati, tenendo conto delle evidenze scientifiche e dell’evoluzione dello scenario epidemiologico.
Alla circolare sono allegati i moduli di consenso al COMIRNATY (BioNTech/Pfizer) e allo Spikevax (Vaccino COVID-19 Moderna)
Ultimo aggiornamento: Mercoledì 15 Settembre 2021, 15:12
© RIPRODUZIONE RISERVATA